產品認證
NRTL稱為國家認可的測試實驗室(NRTL),根㯫美國聯邦法典29 CFR1910.7所認可的,其條例於1988年制定,為北美市場驗證產品的第三方機構。 OSHA (職業安全與健康管理局) 創建NRTL是為了確保某些類型的設備在工作場所得到安全使用的測試和認證又保護勞工安全。在加拿大,只有經過加拿大標準委員會 (SCC)認可的驗證機構才可以進行此項服務。
SCC是加拿大管制電器商品的權威機構,產品在加拿大銷售或者進口到加拿大的電器產品必須經過驗證,並以符合加拿大電器規範設立的技術要求。然而,人們對加拿大市場進入的要求誤以為需要加拿大標準協會(CSA)的測試和驗證。其實,製造商和進口商可以與由加拿大(SCC)標準委員會認可的任何測試實驗室合作,以獲取他們的產品驗證,滿足加拿大電器標準的要求。
2017年5月5日,歐盟官方期刊(Official Journal of the European Union)正式發布了歐盟醫療器械法規(REGULATION (EU) 2017/745,簡稱「MDR」)。MDR將取代Directives 90/385/EEC (有源植入類醫療器械指令)and 93/42/EEC(醫療器械指令)。依據MDR Article 123的要求,MDR於2017年5月26日正式生效,並與2020年5月26日期正式取代MDD(93/42/EEC)和AIMDD(90/385/EEC)。
在新版MDR 2017/745/EU中,更是完善了臨床評估(包括器械售後臨床追蹤)和臨床調查的執行、評估、報告和更新資料的相關要求。對特定III類和IIb類器械,臨床評估報告中要考慮諮詢專家小組的意見;對植入式和III類器械,提出考慮臨床研究;要求臨床評估報告按照售後臨床追蹤所取得的數據進行更新; 針對III類和可植入器械,提出了臨床評估報告更新的頻率;明確證明實質等同性需考慮的特點;要求其與風險管理的相互作用等等。
體外診斷醫療器材(In Vitro Diagnostic Devices,IVD)是指用於疾病或其他狀況之診斷用之試劑、儀器與系統,有別於一般泛指的醫療器材(medical device),主要是指不直接接觸人體,利用取自人體的血液、尿液、其他體液或組織切片等,進行人體外試驗或分析的醫療器材。產品包括: 檢驗儀器設備、檢驗試劑/紙、其他周邊處理儀器設備
CB測試證書是由授權的NCB頒發的正式的CB體系文件,其目的是告知其它的NCB,已測試的產品樣品被認定符合現行要求。CB證書的好處可以轉換多國證書,節省費用和時
間,如果已取得CB測試證書和CB測試報告,可以直接申請其它國家的認證證書。被申請國的認證機構對CB測試證書和報告(包括有關國家差異的報告)進行審查(必要時,需提供少量的樣品),如果審查結果合格,就可以獲得該國認證,而無需按照被申請國的章程和程式規則進行附加測試。
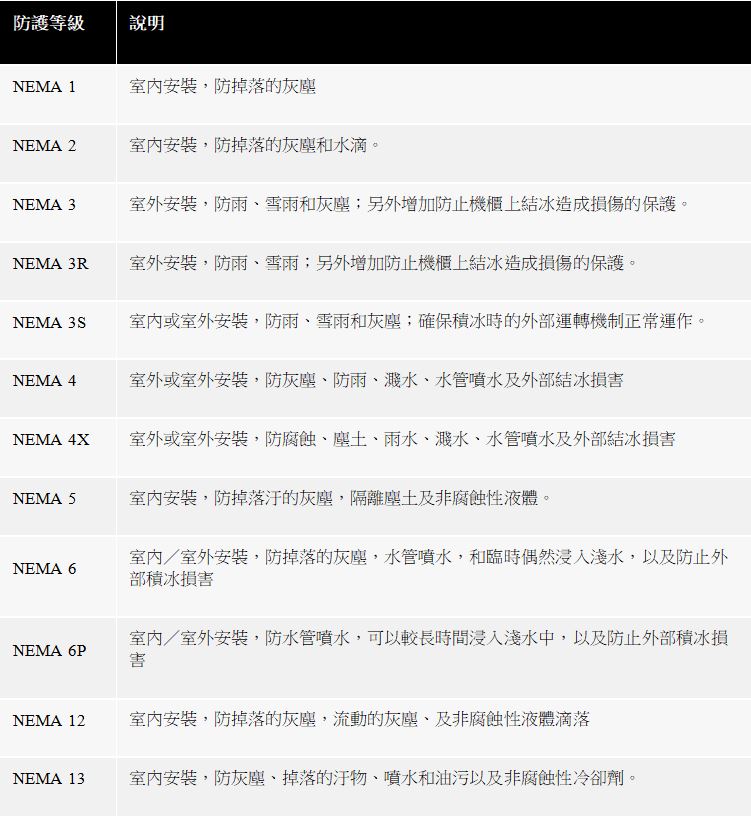
電器製造商協會(National Electrical Manufacturers Association,簡稱 NEMA)一家位於美國華盛頓的技術標準機構,雖然有頒佈大量技術標準,但機構本身並不從事產品核可和認證工作。
以下 NEMA 分類主要介紹用於防止人體意外接觸設備的防護,以及控制櫃外部影響的防護,以稱外殼測試。
IP Rating是國際防護等級認證,又稱異物防護等級或ip代碼,定義了機械和電子設備能提供針對固態異物侵入,液體滲入,意外接觸有何等程度的防護能力。